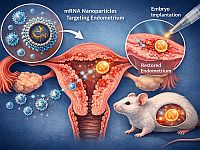
Наночастицы, содержащие мРНК, могут стать эффективным способом лечения бесплодия
Ученые из Института офтальмологии им. Уилмера и Центра наномедицины Медицинского центра Джона Хопкинса предложили новый подход доставки терапевтической мРНК в эндометрий мышей. Они использовали модифицированные липидные наночастицы (ЛНП) – крошечные капсулы из жировых молекул – для доставки мРНК во внутреннюю оболочку матки.
В отчете, опубликованном в журнале Nature Nanotechnology, исследователи отмечают, что в модели повреждения эндометрия их метод улучшал имплантацию эмбриона. Это, по их мнению, открывает перспективу нового подхода к лечению некоторых видов бесплодия. Команда подчеркивает, что их эксперименты демонстрируют возможность целенаправленно доставлять терапевтическую мРНК – молекулярные инструкции, которые клетки используют для синтеза белков и управления своими функциями – в поврежденную слизистую матки на заданный период времени.
Многие гинекологические заболевания, такие как эндометриоз и синдром Ашермана, могут вызывать бесплодие, снижая вероятность прикрепления эмбриона к эндометрию – важнейшему этапу для наступления беременности, даже при применении вспомогательных репродуктивных технологий (ВРТ), включая ЭКО. По словам исследователей, у пациенток, которые не могут забеременеть или выносить ребенка с помощью ВРТ, сейчас нет эффективных методов лечения, одобренных FDA.
Терапия на основе мРНК работает так, что клетки получают инструкции для производства определенных белков без вмешательства в их ДНК. Этот принцип лежит в основе современных методов лечения рака и мРНК-вакцин против COVID-19. При разработке мРНК-терапии одной из главных задач является доставка молекул в нужное место в достаточной концентрации, чтобы добиться эффекта, при этом избегая системной токсичности. В новых экспериментах ученые рассказали, что они поставили целью выяснить, возможно ли доставить нестабильную мРНК прямо в эндометрий с помощью липосомальных наночастиц и какие параметры можно улучшить с их помощью.
Поскольку мРНК быстро разрушается, а клетки содержат ферменты, разрушающие "голую" мРНК, ученые использовали липосомальные наночастицы (ЛНП) для защиты и доставки мРНК, кодирующей иммунный белок GM-CSF (гранулоцитарно-макрофагальный колониестимулирующий фактор). Считается, что GM-CSF помогает улучшить имплантацию, повышая толщину эндометрия. Хотя рекомбинантный белок GM-CSF можно производить в больших количествах, его короткий период действия и риск распределения по другим органам ограничивают его клиническое применение. В первой серии экспериментов ученые вводили мРНК GM-CSF в эндометрий мышей внутриматочно – методом, который уже используется при ВРТ для введения эмбрионов и лекарств. Они обнаружили, что обычные мРНК-ЛНП распространяются за пределы матки и могут вызывать токсическое воздействие на печень и селезенку.
Чтобы снизить риск нецелевой доставки, исследователи модифицировали ЛНП пептидом RGD (аргинилглициласпарагиновая кислота). Этот пептид связывается с интегринами – белками на поверхности клеток, которые активно выражаются в эндометрии в период имплантации (WOI), когда ткань наиболее восприимчива к эмбриону. Такая модификация позволила направить лечение именно в эндометрий, усилить ожидаемый эффект GM-CSF и уменьшить побочные эффекты при введении в период WOI.
После введения специально разработанных мРНК-ЛНП ученые отметили, что уровень белка GM-CSF в эндометрии оставался высоким в течение 24 часов. Через восемь часов он был почти в три раза выше, чем у мышей, получивших рекомбинантный белок. При этом концентрация GM-CSF в крови была в 60 раз ниже, чем при введении рекомбинантного белка, что свидетельствует о лучшей безопасности и меньшем риске повреждения других органов.
Применяя тот же метод на мышиной модели повреждения эндометрия, имитирующей структурные изменения, снижающие фертильность у людей, ученые обнаружили, что имплантация эмбрионов восстановилась до уровня здоровых мышей. У необработанных животных количество мест имплантации было в среднем на 67% меньше. При этом у обработанных мышей не выявили токсического воздействия на матку и другие органы.